CO2と水から石油を作ればベンチャーは大儲け?
我々が石油や石炭を使うことによって、空気中のCO2濃度は着実に増加してきており、これによって地球温暖化が起こっているといわれています。一方、将来石油が枯渇するともいわれています(実際は石油枯渇はずっと先の話ですが… 石油はあと40年で枯渇する? 石油はいったいいつなくなるのか 参照)。
それなら、CO2から石油を作る技術が開発できないか。そうすれば、地球温暖化問題と石油枯渇問題が一挙に解決する。そんなことが可能なのでしょうか。
最近、Yahoo知恵袋にはこのような質問が掲載されました。
CO2(二酸化炭素)と水(水素)で石油(燃料)が作れるという噂がありますが、本当ですか?(それが本当なら)化石燃料がいらなくなるし我が日本は豊かな国になり、生活や暮らしも裕福になれるし、ベンチャー企業が大儲けできるし、大富豪になれることもできるよね?・・・でも世界の石油メジャーや国際資本銀行家たちや、世界各国の政府と政治家たちに激怒されませんか?(質問の文章は一部変更しています)
この質問に対して、私なら「CO2と水から石油を作ることは可能です。しかし、質問者が考えていることとはちょっと違うかもしれません」と答えるでしょう。
人類は無限のエネルギーを手に入れる
では、CO2と水から石油が合成できるとしたら、どんなことが起こるのか、少し詳しく考えてみたいと思います。
まず、石油を燃やすとCO2と水が発生します。(燃やすということは、当然ですが、酸素が必要となります)
石油 + 酸素 → CO2 + 水 …… ①
このとき、大量の熱が出ます。この熱エネルギーを使って私たち人類は発電したり、自動車を走らせたりしているわけです。一方で、石油の燃焼に伴ってCO2や水が発生します。このCO2が大気中に増えた結果、地球温暖化が引き起こされているわけです。
では、このCO2と水から石油が作れるならどうなるか。(このとき、石油ができるだけでなく、CO2と水に含まれる酸素もできてきます)
CO2 + 水 → 石油 + 酸素 …… ②
この反応は可能なのかというのが、前述の知恵袋の質問でした。実は可能なのです。つまり、CO2と水から石油を作ることができる。厄介者と思われていたCO2がこの反応で資源になるのです。
であれば、こういう装置を作ってみたらどうでしょうか。この装置をX装置と呼ぶことにしましょう。
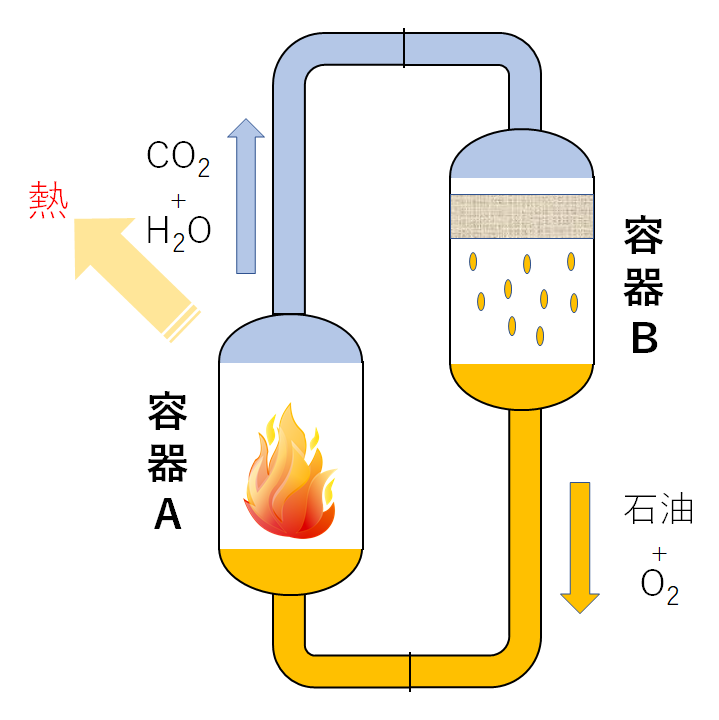
まず、このX装置では容器Aでは石油を燃やします。つまり①の反応が起こることになります。そのとき、CO2と水が発生します。このCO2と水を容器Bに送って式②を行わせます。つまり、CO2と水から石油を作るのです。
すると、容器Bでは石油と酸素ができますから、これを再び容器Aに送って、燃やします。するとCO2と水ができるので、また容器Bに送ります。・・・
この循環は式②が可能と考えれば、原理的に無限に続けることができます。
そして、容器Aでは石油が燃えているのですから、当然、熱が出ます。その熱を使ってボイラーで蒸気を作ってタービンを回せば発電することできます。あるいはこの装置ごと車に乗せて、発生した熱でピストンを動かせば永久に走り続ける車を作ることができます。
やったー! われわれ人類はついに無限のエネルギーを手に入れたぞ!
と、無限のエネルギーを手に入れたところで、では、このX装置でわれわれはどのくらいのエネルギーを手に入れることができるのか、計算してみましょう。
その技術を発明したベンチャーは儲かるのか
CO2と水から石油を作ることができれば、必然的にX装置を作ることができます。では、この技術を発明したベンチャー企業はどのくらい儲かるのでしょうか。
それを知るためには、このX装置でどのくらいエネルギーが生み出されるのかを見積もっておく必要があるでしょう。例えX装置が完成しても、発生するエネルギーがわずかであればそんなに大儲けはできません。
発生する熱エネルギーについては「ヘスの法則」によって計算することができます。
ヘスの法則とは
反応熱 = 生成物の生成熱の総和 - 反応物の生成熱の総和
という計算式で化学反応によって発生あるいは消費される熱(反応熱)を計算することができるという法則です。
つまり、「何を原料にしたか」(反応物)ということと、「何ができたか」(生成物)ということが分かれば、あとは、発生する熱量を計算によって求めることができるのです。
※ヘスの法則は高校化学で習います。もし読者の方で受験生の方がいらっしゃるのなら、大学の試験問題に出る可能性がありますので、ついでに覚えてしまいましょう。
では、容器Aの反応熱を計算してみましょう。ただし、計算が複雑になるので、ここではメタンCH4(都市ガスの主成分)を燃やすことにしましたが、考え方は石油の場合と同じです。
CH4 + 2O2 → CO2 + 2H2O
計算の結果、容器Aで発生する熱エネルギーは890.3 kJ/molとなりました。
(計算方法の詳細は、この記事の最後に書いていますので、参照してください)
つまり、容器Aではメタン1モル(メタン1モルは22.4リットル、重さなら16gです)あたり890.3kJの熱が発生することになります。これは常温(20℃)の水なら約2.7リットルを沸騰させることができる熱量です。これはなかなかの量ですね。
では、容器Bの反応熱はどうなるのでしょうか。
容器Bの反応式は次のようになります。
CO2 + 2H2O → CH4 + 2O2
つまり容器Bでは容器Aとは逆に、CO2と水からメタンCH4と酸素ができることになります。
計算の結果、容器Bで発生する熱エネルギーは-890.3 kJ/molとなりました。
おやっと思われた方もいらっしゃるかもしれません。容器Aの場合と同じ数値じゃないかと。これは当然で、容器Bでは、容器Aとは逆の反応が起こっているからです。つまり、反応物(原料)と生成物(できたもの)の生成熱の総和が入れ替わっているだけなのです。
ヘスの法則は「原料が何か」と「何ができたか」だけで計算するので、容器Bの反応熱の数値も容器Aの場合と同じになります。
ただし、記号が容器Aではプラスだったものが容器Bではマイナスになっているところが違います。
では、マイナスの反応熱というのはどういうことなのでしょうか。
これは吸熱反応といって、熱を吸収する反応を意味します。実際に容器BでCO2と水から石油を作る反応を行うと熱を吸収します。すると、容器の温度がどんどん下がって行って、反応が進まなくなってしまいます。
容器Bの反応を進めるためには、外部から熱を加えてやって温度を一定に保つ必要があります。そのために必要な熱量が890.3 kJ/molというわけ。そして、この熱量は、容器Aで石油を燃やした時と同じ熱量になる。というのがヘスの法則からの結論です。
つまり、X装置でCO2と水から石油を作ろうとすると、熱エネルギーが必要となり、その熱エネルギーを確保するために、作られた石油をすべて燃やさなければならないということなのです。
実際には、熱が外部に逃げてしまう。つまり熱のロスがありますので、作られた石油をすべて燃やしてもまだ、CO2から石油はつくれません。もっとエネルギーが必要となります。
ということで、このX装置からエネルギーを取り出すことはできませんし、石油を取り出すこともできません。残念ながら、われわれ人類は無限のエネルギーを手に入れたわけではないのです。( 水や空気で走る車がすでに実用化されている? 参照)
CO2と水から石油はできるという投資話は要注意
なお、ここでは、ヘスの法則で説明しましたが、一般には熱力学第一法則で説明されます。熱力学第一法則とは簡単に言えば「(第一種)永久機関は不可能である」ということです。
ここで取り上げたX装置から熱または石油を取り出すことができれば、X装置は永久機関ということになりますが、熱力学第一法則は永久機関を禁止していますので、熱エネルギーも石油も取り出すことはできない(もし取り出すと、X装置は止まってしまう)ということなのです。
実は1980年代にCO2による地球温暖化が問題になり始めたころから、CO2を原料として燃料を作れないかという話がありました。CO2が地球温暖化の原因となるのなら、CO2を捕まえてきて、また燃料にすればいい。一応だれでも考えることです。
実際に、当時多くの化学者たちがCO2から燃料を作ろうといろいろなアイデアを発表してきました。でも、実用化には至りませんでした。当たり前ですよね。ヘスの法則を使って計算したように、CO2から燃料を作ると、作った燃料より多くの燃料を必ず燃やさなければならなくなるからです。
このヘスの法則は高校時代に化学の時間に習ったはずなのに、実際には多くの学者先生がCO2から燃料を作ろうといろいろと努力をなされました。いずれも失敗しましたけどね。
今でもときどき、「これはヘスの法則に反するだろう」という反応を持ち出して事業化しようとする方もいらっしゃるようで、先日も私の友人から、そんな怪しげな投資話の相談を受けたことがあります。これはヘスの法則に反するので実現できませんよと説明しました。
2020年11月23日
【付録】X装置での反応熱の計算
1.ヘスの法則とは
反応熱 = 生成物の生成熱の総和 - 反応物の生成熱の総和
という計算式で化学反応によって発生あるいは消費される熱(反応熱)を計算することができるという法則です。
2.容器Aの反応熱
容器Aの反応を次のように考えます。
CH4 + 2O2 → CO2 + 2H2O
容器Aでは石油を燃やすのですが、計算が複雑になるので、ここではメタンCH4(都市ガスの主成分)を燃やすことにしましたが、考え方は石油の場合とおなじです。
(石油の化学式は一般にCnH2n+2で表されますが、メタンは石油の化学式のn=1の場合と考えることができます)
ちなみに生成熱というのは、物質1モルがその成分元素の単体から生成するときの反応熱のことを言いますが、難しく考えずに、物質それぞれが持っている固有の数値と考えてください。それぞれの物質の生成熱は実測されていて一覧表となっています。
反応物(原料)側
メタン(CH4) 生成熱=74.8kJ/mol、モル数=1
酸素(O2) 生成熱= 0.0kJ/mol、モル数=2
生成熱の総和 = 74.8 × 1 + 0.0 × 2 = 74.8 kJ/mol
生成物(できたもの)側
二酸化炭素(CO2) 生成熱=393.5kJ/mol、モル数=1
水(H2O) 生成熱=285.8kJ/mol、モル数=2
生成熱の総和 = 393.5 × 1 + 285.8 × 2 = 965.1kJ/mol
容器Aの反応熱 = 生成物側の生成熱の総和―反応物側の生成熱の総和
= 965.1 ― 74.8 = 890.3 kJ/mol
3.容器Bの反応熱
容器Bの反応熱を計算します。
容器Bの反応は次のようになります。
CO2 + 2H2O → CH4 + 2O2
つまり容器BではCO2と水からメタンCH4ができることになります。
反応物(原料)側
二酸化炭素(CO2) 生成熱=393.5kJ/mol、モル数=1
水(H2O) 生成熱=285.8kJ/mol、モル数=2
生成熱の総和 = 393.5 × 1 + 285.8 × 2 = 965.1kJ/mol
生成物(できたもの)側
メタン(CH4) 生成熱=74.8kJ/mol、モル数=1
酸素(O2) 生成熱= 0.0kJ/mol、モル数=2
生成熱の総和 = 74.8 × 1 + 0.0 × 2 = 74.8 kJ/mol
容器Bの反応熱 = 生成物側の生成熱の総和―反応物側の生成熱の総和
= 74.8 ― 965.1 = -890.3 kJ/mol
【関連記事】
CO2を増やさない合成燃料 e-fuelとは何か × アウディ、ポルシェ、トヨタも参入
グリーンイノベーション 再生可能な合成燃料(ディーゼル、ジェット)の開発戦略
石油が枯渇したらジェット機は飛べなくなるのか…温室効果ガスゼロ時代のジェット燃料
2050年に温室効果ガス排出実質ゼロ…あなたが次に買う未来の自動車はこうなる
世界燃費の悪い車をランキングしてみたら驚きの結果が…あの名車がつぎつぎと
グリーン水素でなければ意味がない―環境省の水素ステーションは地球に優しくなかった
石油はあと40年で枯渇する? 石油はいったいいつなくなるのか
水素は海水からとりだせば無尽蔵のエネルギー源になる?
水や空気で走る車がすでに実用化されている?
アメリカ海軍は海水から燃料を取り出す技術を開発した?



特殊光触媒を用いた人工石油の製造実験がが報道されました。
しかし検索してもこのブログがトップに来ています。
このブログ内容について修正又は削除が必要ではないでしょうか。
個人的にはこのプログは原理としての話をしているのであって、エネルギー資源の生成の話としてはもっと煮詰めようがあると思います。間違った内容ではないので修正または追記をお願いしたいです。
匿名さん。コメントありがとうございます。
この記事では、CO2や水から石油を作ることはできるが、その石油を燃やして得られるエネルギーよりも多くのエネルギーが必要となることをヘスの法則から導き出しています。この関係は特殊光触媒を使おうが、紫外線を当てようが、ナノバブルを使おうが変わりません。結論は同じです。
大阪鶴見公園で行われた公開実験のことを仰っているのだと思いますが、これが報道のとおりだとするとヘスの法則に反する。つまり永久機関だということです。まさに私が言っている「こういう投資話には要注意」の典型的な例だと思います。
こういう話は時々出ては消えていきます。まあ1年もたてば、みんな忘れて、だれも相手にしなくなっているでしょう。逆に本物なら、ノーベル賞は確実っていうか、現代の科学がひっくり返ってしまうでしょう。どっちになるか1年ほど待てばわかることです。